초록
비타민 D의 고전적인 기능은
칼슘-인 항상성을 조절하고
뼈 대사를 조절하는 것입니다.
그러나 비타민 D 결핍은 당뇨병, 천식 및 류마티스 관절염과 같은 염증 증가 및 면역 체계의 탈조절과
관련된 여러 만성 질환에서 보고되었습니다.
이러한 관찰은 실험 연구와 함께 면역 기능 조절에서 비타민 D의 중요한 역할을 시사합니다.
이것은 비타민 D 대사의 질병별 변화에 대한 가설로 이어지며 건강한 면역 체계를 유지하는 데 있어
비타민 D의 역할을 강화합니다.
두 가지 주요 관찰은 비타민 D의 이 중요한 비고전적 작용을 입증합니다.
첫째, 비타민 D 수용체(VDR)는 B 및 T 림프구, 단핵구, 대식세포 및 수지상 세포를 포함한 대다수의 면역 세포에서 발현됩니다.
1,25(OH) 2 D 3란 활성 형태로 변환합니다.
둘째, 비타민 D와 VDR 신호는 함께 자가면역과 항염증 효과에 대한 억제 역할을 하여 수지상 세포 및 조절 T 세포 분화를 촉진하고 T 헬퍼 Th 17 세포 반응과 염증성 사이토카인 분비를 감소시킵니다.
이 리뷰는 비타민 D의 잠재적인 면역 조절 특성에 대한 실험 데이터와 임상 관찰을 요약합니다.
키워드: 비타민 D ; 면역 체계 ; 장내 미생물 ; 자가면역질환 ; T 세포
1. 소개
인산칼슘 항상성 조절과 골 회전율 조절에서
비타민 D의 역할은 잘 알려져 있습니다.
비타민 D 상태는 성장기의 골격 건강에
상당한 영향을 미치며, 성장기의 결핍은
구루병[ 1 ]을 유발하는 반면,
성인기의 비타민 D는 골연화증과 다양한 정도의
골다공증 연화증[ 2 ]을 유발합니다.].
낮은 비타민 D 상태는 골 회전율을 증가시키고
골밀도를 감소시키며 골절 위험 증가와 관련이 있습니다.
지난 20년 동안 골격 건강에 대한 잘 알려진 효과 외에도 비타민 D 수용체(VDR)와 비타민 D 활성화 효소 1 -α-수산화효소(CYP27B1)는 장, 혈소판, 췌장, 전립선 등 뼈와 신장 외부의 여러 세포에서 발현됩니다[ 3 ].
면역 기능에 관여하는 여러 세포가 VDR과 CYP27B1을 발현하는데, 이 관찰은 비타민 D의 활성 형태인 1,25(OH) 2 D 3가 다양한 수준에서 면역 기능을 제어할 수 있습니다.
면역 체계의 조절에서 비타민 D의 역할에 대한 이전 리뷰 는 최근 몇 년 동안 발표되었습니다[ 4,5 ] .
여기에서 우리는 실험 및 임상 분야 모두에서 저자의 전문성을 바탕으로 최근 증거를 요약합니다.
2. 비타민 D 대사
비타민 D는 식이 섭취를 통해 체내로 들어가거나
(비타민 D 3 의 약 20%는 식이와 함께 가정됨)
UVB 노출 후 7-디하이드로콜레스테롤로부터 피부(80%)에서 합성됩니다.
비타민 D 3 는 효소 시토크롬 P450 2R1(CYP2R1) 및 시토크롬 P450 27(CYP27A1)에 의해 25(OH)D 3로 간에서 수산화 됩니다 .
완전 활성 대사 산물인 1,25(OH) 2 D 3 는
효소 CYP27B1, 파라토르몬(PTH) 및 섬유아세포 성장 인자 23(FGF-23)에 의해 신장에서 수산화되어
CYP27B1 합성 및 활성을 조절합니다[ 6 ].
1,25(OH) 2 D 3 합성 1,25(OH) 2 D 3 및 FGF-23의 높은 수준은 CYP27B1을 억제하고
시토크롬 P45024A1(CYP24A1)을 유도하여 1,25(OH) 2 D 3 는 비활성 형태 24(OH)D 3가 됩니다.
[ 7 ].
신장 외에도 CYP27B1은 면역 세포를 포함한
다른 세포 유형에서 발현됩니다.
이 세포는 자가분비 및/또는 측분비 효과가 있는 1,25(OH) 2 D 3 를 생성하며,
국소적으로 생성된 높은 수준은
면역 조절을 담당하는 것으로 생각됩니다.
면역 세포에서 CYP27B1 합성의 조절은 1,25(OH) 2 D 3 의 신장 생성을 조절하는 신호와 다릅니다 .
지질다당류(LPS) 및 사이토카인과 같은 염증 신호는 CYP27B1의 단핵구 및 대식세포 생성을 유도합니다[ 8 , 9 , 10 ].
1,25(OH) 2 D 3 조절의 이러한 차이점 생산 지점은
면역 조절로서 자가분비/주변분비 효과를 나타냅니다.
3. 비타민 D 상태
비타민 D 상태는 하이드록실화 형태 25(OH)D 3 의
혈액 측정에 의해 정의 되지만
바람직한 비타민 D 수준을 식별하기 위한
임계값 수준에 대한 공통된 합의는 없습니다.
여러 과학 학회와 여러 국가의 지침에서는 비타민 D 충분량을 고려하기 위해 50nM/L 또는 75nM/L을 설정했지만[ 11 , 12 , 13 ],
일반적으로 25(OH)D 3 수준이 50 nM/ L 미만은
성인의 골 대사 변화, 낙상의 위험 증가 및 근육병증과 관련이 있습니다[ 14 , 15 , 16 , 17 , 18 ].
해당 분야의 전문가들은 일반적으로 25(OH)D를 유지하는 데 동의합니다.3
독성 효과 없이 특정 골격 효과를 얻기 위해 20~125nM/L 사이 이어야 합니다.
최근 문헌 에서는 50,000 IU 이상의 비타민 D
3 bolus 투여가 낙상 및 골절 위험을 증가시킬 수 있다는 의혹을 제기합니다 [ 19 , 20 ]. 또한 25(OH)D 3 와 관련된 사망률 은 "U자형 곡선"이며
150nM/L보다 높은 25(OH)D 3 수준은 사망률 증가와 관련이 있습니다[ 21 ].
4. 비타민 D와 선천 면역 체계: 항균 활성
선천 면역 체계는 감염에 대한 첫 번째 방어 체계이며, 침입하는 병원체에 대해 신속하게 싸워야 합니다.
선천성 면역 체계는 숙주와 상주 미생물(미생물총)의 구성 요소를 모두 이해합니다. 숙주 방어는 감염에 대한 물리적 장벽(피부, 점막 표면, 점액 및 혈관 내피 세포), 상피 및 식세포에서 발현되는 효소(리소자임), 항균 펩타이드 및 단백질(디펜신, 카텔리시딘 및 기타 식세포에서 발현), 염증성 체액 성분(보체 및 옵소닌), 병원체를 빠르게 인식하는 세포 수용체(톨 유사 수용체) 및 세포 성분(비만 세포, 수지상 세포, 대식세포, 호중구 세포 및 자연 살해자)을 포함합니다.
미생물군 비타민 D 간의 상호 작용은 다음 단락에서 분석됩니다.
비타민 D는 선천성 면역의 잘 알려진 조절자입니다.
이 주제에 대한 첫 번째 데이터는 결핵 및 나병과 같은 마이코박테리아로 인한 질병의 치료에 대해 생성되었지만 [ 22 , 23 ] 이러한 작용을 담당하는 기전은 다음과 같습니다. 최근 몇 년 동안 해명되었습니다.
1,25(OH) 2 D 3 는 대식세포와 단핵구와 각질세포에서
데펜신 β2와 카텔리시딘 항균 펩타이드(CAMP)의 생성을 증가시켜 항균 활성을 증가시킵니다[ 24 , 25 , 26 ].
또한, 1,25(OH) 2 D 3 는 선천성 면역 세포의 화학주성, 자가포식 및 포식용해체 융합을 증가시킵니다[ 27, 28 ].
M. tuberculosis 와 같은 병원체에 대한 인간 단핵구의 노출은 CYP27B1 및 VDR의 발현을 상향 조절하여
감염 부위에서 1,25(OH) 2 D 3 를 생성하는
세포 능력을 향상시키고 이 대사 산물에 반응합니다. 그러나 대식세포는 기능이 다르며 이질적입니다[ 29 ].
인터루킨(IL)-15 자극 후에 형성된 대식세포는 비타민 D 자극에 반응하여 항균 활성을 증가시키는 반면, IL-10으로 자극 후에 얻은 식세포 대식세포는 높은 식세포 활성에도 불구하고 비타민 D 수준에 약하게 영향을 받습니다[ 10 , 30 ].
1,25(OH) 2 D 3 는 단핵구/대식세포뿐만 아니라 케라티노사이트, 상피세포, 장세포, 폐세포, 각막세포 등 선천성 면역계에 1차 방어막으로 참여하는 다른 세포에서도 CAMP를 상향 조절합니다.
및 태반 영양막(포괄적인 검토를 위해 참조 Wei and Christakos, 2015) [ 4 ].
마이코박테리아 이외의 감염에 대한 인간의 데이터는 요로 및 호흡기 감염과 패혈증에 대해 생성되었습니다.
CAMP 생성 감소와 β2 방어로 인해 비타민 D 수치가 낮은 어린이의 요로 감염 소인은 연관 연구에 의해 제안되었습니다[ 31 , 32 ]. 또한 만성 폐쇄성 폐질환(COPD) 환자의 CAMP 및 기타 항균성 펩타이드 수치는 급성 악화 위험 증가와 관련이 있었습니다[ 33 ].
이 데이터와 일치하게 1,25(OH) 2 D 3 를 사용한 치료 는 CAMP(항균펩타이즈)의 발현 증가와 염증성 사이토카인 조절 덕분에 천식 환자의 호흡기 감염을 줄이는 데 효과적이었습니다[ 34].
패혈증에서 비타민 D 상태와 비타민 D 보충의 역할에 대한 데이터는 소아와 성인 환자 모두에서 사용할 수 있습니다. 소아 환자에서는 25(OH)D 3 및 CAMP의 명확한 역할이 입증되지 않은 반면[ 35 ], 성인에서는 패혈증에서 낮은 수준의 25(OH)D3 가 발견되었고[ 36 ] 고용량의 비타민 D3는 순환하는 CAMP를 증가시키고 IL-6 및 IL-1β와 같은 염증성 사이토카인을 감소시킵니다[ 37 ].
보다 최근에 HIV 감염에 대한 내성을 증가시키는 데 비타민 D의 가능한 역할에 대한 데이터가 발표되었으며, 특히 HIV에 노출된 혈청 음성인 개인은 구강 점막과 말초 혈액에서 더 많은 CAMP를 생산하고
질 점막에서 더 높은 CYP24A1 mRNA를 가집니다.
CYP24A1은 높은 수준의 1,25(OH) 2 D 3 [ 38 ]의 지표로 간주됩니다. 낮은 혈청 비타민 D는 HIV/AIDS 진행 및 사망률과 관련이 있습니다[ 39 ].
1,25(OH) 2 D 3 는 β2-4를 방어하는 것과 같은
다른 항균성 펩타이드의 생산을 증가시킬 수 있습니다.
이 능력은 시험관 내에서 단핵구 자극에 의해 입증되었으며[ 40 , 41 ]
소아 환자의 생체 내에서 모두 입증되었습니다. 피 [ 32 ].
비타민 D는 선천성 면역 체계를 조절할 수 있으며,
또한 면역 세포에 대한 식세포 능력을 증가시키고 [ 42 , 43 ]
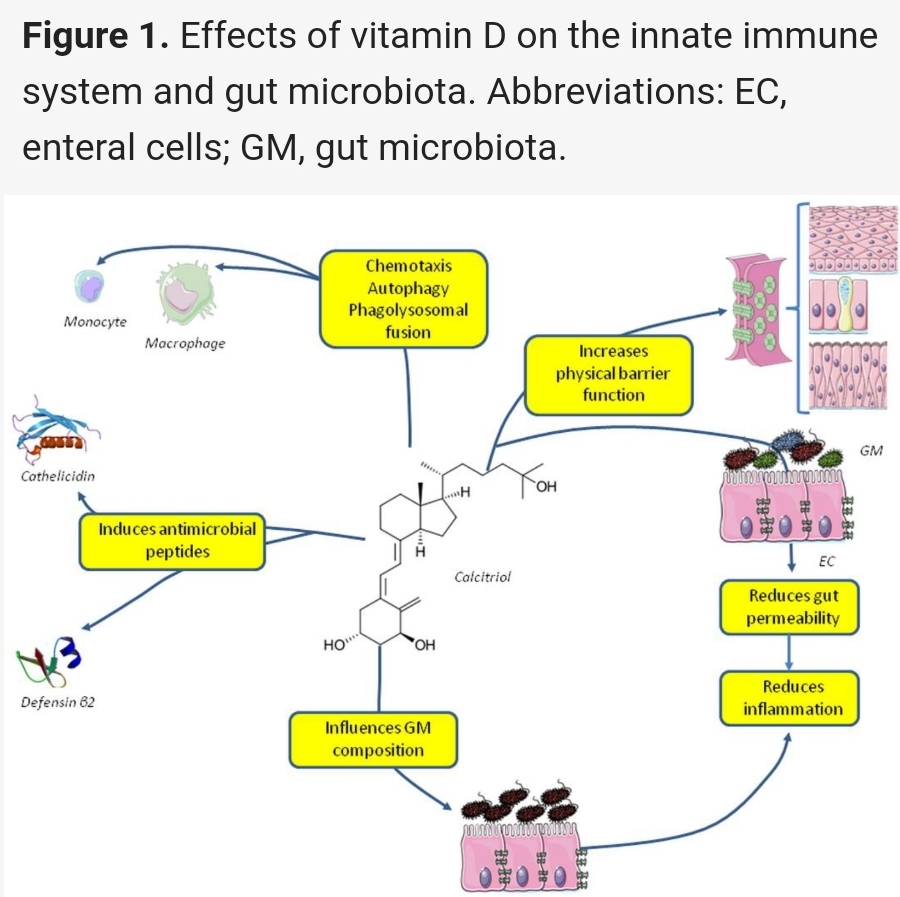
상피 세포의 물리적 장벽 기능을 강화합니다. 특히 1,25(OH) 2 D 3 는 각막 [ 44 ] 및 장 [ 45 ] 상피 장벽 기능을 향상시킬 수 있습니다( 그림 1 ).
회원에게만 댓글 작성 권한이 있습니다.